Células madre: solo existen dos tratamientos clínicamente aprobados
La Comisión Asesora en Terapias Celulares y Medicina Regenerativa del Ministerio de Ciencia, Tecnología e Innovación Productiva, informa sobre los tratamientos establecidos y advierte sobre otros que no presentan evidencia terapéutica comprobada.
El Ministerio de Ciencia, Tecnología e Innovación Productiva, a través de la Comisión Asesora en Terapias Celulares y Medicina Regenerativa, desea dar a conocer los aspectos más relevantes en el campo de las investigaciones con células madre. Las mismas poseen dos características distintivas: son células no especializadas que se renuevan ilimitadamente; y bajo ciertas condiciones fisiológicas o experimentales, se las puede inducir a que se conviertan en células con funciones especiales, por ejemplo: células musculares cardíacas o células pancreáticas para la producción de insulina.
Los científicos trabajan mayormente con dos clases de células madre de animales y de seres humanos: las embrionarias y las adultas. Las células madre embrionarias pueden convertirse en cualquier tipo de célula del cuerpo, mientras que las adultas generan los mismos tejidos del órgano en el cual residen.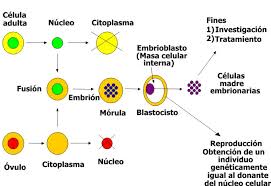
En la década del 60, los investigadores descubrieron que la médula contenía por lo menos dos clases de células madre adultas: hematopoyéticas, que formaban todos los tipos de células sanguíneas del cuerpo; y medulares estromales o mesenquimales, que comprendían una población mixta capaz de desarrollar células del hueso, cartílago, grasa y tejido conectivo fibroso.
Existen dos tratamientos con células madre aprobados por los organismos de control debido a su eficacia terapéutica y a que no han presentado riesgos secundarios indeseables: el transplante alogénico de células madre de médula ósea, sangre periférica y cordón umbilical; y el autotrasplante de células madre de médula ósea y sangre periférica para tratar enfermedades curables con trasplante de células progenitoras hematopoyéticas. Fuera de estos tratamientos, no existe evidencia clínica reproducible y contundente, ni tratamientos establecidos a nivel nacional e internacional, que hayan demostrado la eficacia del autotransplante de células madre de médula ósea o cordón umbilical para mejorar o curar enfermedades altamente discapacitantes. Los únicos tratamientos establecidos son aquellos destinados a enfermedades que se curan con trasplante de médula ósea y por ello son los únicos que se realizan con éxito en miles de pacientes.
Recientemente, la Administración de Drogas y Alimentos de Estados Unidos (FDA), emitió un comunicado expresando su preocupación por la oferta creciente de tratamientos ilegales y potencialmente dañinos en ese país. La institución ratificó allí la necesidad de contar con estudios clínicos que demuestren la seguridad y efectividad de otro tipo de tratamientos. En tal sentido, el comunicado también advirtió sobre los tratamientos ofrecidos en otros países, ya que en la mayoría de los casos, las intervenciones no cuentan con un protocolo médico que las respalde.
En la investigación clínica que involucran el uso de células madre deben ser aprobados por el Instituto Nacional Central Único Coordinador de Ablación e Implante (INCUCAI). Es importante destacar que las prácticas experimentales deben realizarse bajo un marco regulatorio estatal que compruebe su eficacia terapéutica y la ausencia de efectos secundarios indeseables.
En los últimos tiempos se ha incrementado la oferta de tratamientos de autotrasplante de células madre para tratar enfermedades como: las parálisis por lesiones cerebrales o de la médula espinal, las neurodegenerativas como la enfermedad de Parkinson o trastornos metabólicos como la diabetes. En algunos casos se trata de procedimientos experimentales que deben demostrar su eficacia y seguridad en seres humanos, por lo que deben contar con un protocolo aprobado y sin costo para el paciente, quien debe ser informado del carácter experimental del tratamiento. A su vez, algunas instituciones que los ofrecen se presentan ante potenciales pacientes y a sus familiares con promesas irrealizables de curación y mejora de las enfermedades, a pesar de que la evidencia señala que muchas de las prácticas ofrecidas no poseen efectos terapéuticos comprobados ni siquiera en modelos animales.
La Comisión Asesora en Terapias Celulares y Medicina Regenerativa promueve la difusión de información de calidad sobre los tratamientos con células madre aprobados, con el objetivo de evitar la exposición de pacientes a intervenciones experimentales y potencialmente peligrosas para su salud. Donde esta la farsa ??
Donde esta la farsa ??  En los periódicos y noticieros es cada vez más frecuente encontrarse con una familia que apela a la solidaridad de la población para recaudar fondos para poder hacer frente a un costoso tratamiento con células madre en China que necesita realizarse un pariente o un amigo. Se organizan campañas de donación voluntaria, festivales, sorteos o recitales con artistas y personalidades de la farándula; todo para juntar los muchos dólares que son necesarios para costear la terapia. En estos casos, la desesperación y la urgencia de los familiares por ver una mejora en la salud de su ser querido, puede hacerlos caer en la trampa de quienes ofrecen la promesa de un tratamiento cuya efectividad no ha sido probada y cuya inocuidad tampoco ha sido discutida.
En los periódicos y noticieros es cada vez más frecuente encontrarse con una familia que apela a la solidaridad de la población para recaudar fondos para poder hacer frente a un costoso tratamiento con células madre en China que necesita realizarse un pariente o un amigo. Se organizan campañas de donación voluntaria, festivales, sorteos o recitales con artistas y personalidades de la farándula; todo para juntar los muchos dólares que son necesarios para costear la terapia. En estos casos, la desesperación y la urgencia de los familiares por ver una mejora en la salud de su ser querido, puede hacerlos caer en la trampa de quienes ofrecen la promesa de un tratamiento cuya efectividad no ha sido probada y cuya inocuidad tampoco ha sido discutida.
La Administración de Alimentos y Medicamentos (FDA) se mostró preocupada por la oferta de tratamientos con células madre ilegales y potencialmente dañinos para la salud. Así fue que en enero de 2012, la FDA sacó una nota de prensa donde advierte sobre los tratamientos con células madre tanto en los EE.UU. como en el resto del mundo.
 |
La FDA alerta por el auge de tratamientos ilegales y potencialmente dañinos que se ofrecen tanto en los EE.UU., como en otros países. También, menciona que cualquier otro tipo de tratamiento debe contar con estudios clínicos que muestren su seguridad y su eficacia, del mismo modo que las intervenciones necesitan el aval de un protocolo médico. Existen numerosos institutos privados que promueven tratamientos con células madre para tratar enfermedades tales como la diabetes, Parkinson, parálisis de la médula espinal, etc; tratamientos que se encuentran en fase experimental y que todavía no se ha demostrado que resulten ser seguros y eficaces en humanos. En cualquier caso, el paciente tiene que estar informado de que la terapia que se le está aplicando se encuentra en fase experimental, la cual debe contar con un protocolo aprobado por el organismo competente y no debe tener costo alguno para la persona tratada.
La FDA aconseja:
Si piensa someterse a un tratamiento con células madre en EE.UU., consulte a su medico si ese tratamiento cuenta con la aprobación de la FDA o si Ud. va a participar de un estudio clínico supervisado por la FDA aun si las células son suyas, ya que pueden generarse riesgos cuando se manipulan las células luego de su extracción. Existe riesgo potencial cuando las células se transfieren a un área donde no tienen la misma función biológica que cumplían en su ubicación original en el cuerpo. Las células que se ubican en otro lugar del organismo pueden multiplicarse, formar tumores o pueden migrar a otras zonas del cuerpo.
Si piensa someterse a un tratamiento con células madre en otro país, recabe toda la información posible acerca de las políticas que regulan estos tratamientos en ese país. Sea precavido y tome las medidas necesarias antes de tratarse con un medicamento a base de células madre en aquellos países donde, a diferencia de los EE.UU., no se exigen estudios clínicos previos que indiquen si el medicamento es seguro y efectivo. La FDA solamente reglamenta el uso de tratamientos con células madre en los Estados Unidos y, por tanto, no posee suficiente información acerca de los establecimientos en el exterior que elaboran los medicamentos para tales fines.

No hay comentarios:
Publicar un comentario